Trộn hai thể tích bằng nhau của dung dịch HNO 3 và dung dịch NaOH có cùng nồng độ mol/l. Giá trị pH của dung dịch sau phản ứng là
A. pH = 2.
B. pH = 7.
C. pH > 7.
D. pH < 7.
Trộn hai thể tích bằng nhau có cùng nồng độ mol của dung dịch H2SO4 và dung dịch NaOH thì pH của dung dịch sau phản ứng:
A. <7
B. =7
C. >7
D. không xác định được
Đáp án A
Dung dịch H2So4 và NaOH có cùng V, cùng CM nên số mol chất tan bằng nhau
2NaOH + H2SO4→ Na2SO4+ 2H2O
X mol X mol
Do đó NaOH hết, H2SO4 dư. Dung dịch sau phản ứng có pH <7
Trộn 300ml dung dịch có pH = 2 gồm HCl và HNO3với 300ml dung dịch NaOH nồng độ a (mol/l) thu được 600 ml dung dịch có pH = 11. Giá trị của a là:
A. 0,012
B. 0,021
C. 0,018
D. 0,024
Đáp án A
pH = 11 => OH- dư sau phản ứng => pOH =3
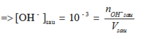
=> nOH- sau = Vsau . [OH-] = 10-3. 0,6= 0,0006 = 6.10-4 (mol)
pH = 2 => [H+]= 10-2 = 0,01M => nH+= 0,3 . 0,01= 0,003
nOH- = 0,3.a
H+ + OH- → H2O
Ban đầu: 0,003 0,3.a
Phản ứng: 0,003 0,003
Sau: 0 0,3.a-0,003
nOH- sau= 6.10-4 = 0,3a -0,003 => a=0,012M
Trộn 100ml dung dịch có pH =1 gồm HCl và HNO3 với 100ml dung dịch NaOH nồng độ a mol/l thu được 200ml dung dịch có pH=12 giá trị của a là
Dung dịch axit ban đầu có [H+] = 0,1 M
⇒ nH+= 0,1.0,1 = 0,01 mol
Dung dịch sau phản ứng có pH = 12
⇒ dư bazơ và có pOH =14 – 12 = 2
⇒ [OH-] = 0,01M
⇒ nOH− dư = 0,002 mol
Phản ứng trung hòa:
nH+phản ứng = nOH−phản ứng = 0,01 mol
⇒ nNaOH ban đầu = nOH−phản ứng + nOH− dư
= 0,01 + 0,002 = 0,012 mol
⇒ a = 0,12M
Trộn 100 ml dung dịch có pH = 1 gồm HCl và HNO3 với 100 ml dung dịch NaOH nồng độ a mol/l thu được 200 ml dung dịch có pH = 12. Giá trị của a là
A. 0,03
B. 0,30
C. 0,15
D. 0,12
Trộn 100 ml dung dịch có pH = 1 gồm HCl và HNO3 với 100 ml dung dịch NaOH nồng độ a mol/l thu được 200 ml dung dịch có pH = 12. Giá trị của a là
A. 0,03
B. 0,30
C. 0,15
D. 0,12
Trộn 100 ml dung dịch có pH = 1 gồm HCl và HNO3 với 100 ml dung dịch NaOH nồng độ a mol/l thu được 200 ml dung dịch có pH = 12. Giá trị của a là
A. 0,03.
B. 0,30.
C. 0,15.
D. 0,12.
Đáp án D
Dd axit ban đầu có [H+] =0,1 M → nH+=0,1.0,1 =0,01 mol
Dd sau phản ứng có pH = 12 → dư bazo và có pOH =14-12=2 → [OH-] =0,01M→ nOH = 0,002 mol
PTHH: H+ + OH- → H2O
Ta có nNaOH = nH+ + nOH dư = 0,01 + 0,002 = 0,012 mol → a = 0,12M
Trộn 300ml dung dịch HCl 0,05M với 200ml dung dịch Ba(OH)2 nồng độ a mol/l thu được 500ml dung dịch có pH = x. Cô cạn dung dịch sau phản ứng thu được 1,9875 gam chất rắn. Giá trị của a và x lần lượt là
![]()
![]()
![]()
![]()
Trộn 300ml dung dịch HCl 0,05M với 200ml dung dịch Ba(OH)2 nồng độ a mol/l thu được 500ml dung dịch có pH = x. Cô cạn dung dịch sau phản ứng thu được 1,9875 gam chất rắn. Giá trị của a và x lần lượt là
A. 2 , 5 . 10 - 3 M ; 13
B. 2 , 5 . 10 - 3 M ; 12
C. 0 , 05 M ; 13
D. 0 , 05 M ; 12
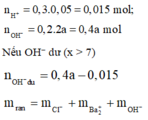
→ 0,015.35,5 + 0,2a.137 + 17(0,4a - 0,015) = 1,9875
→ a = 0,05 M

Đáp án D
Trộn 3 dung dịch H2SO4 0,1M; HNO3 0,2M; HCl 0,3M với những thể tích bằng nhau thu được dung dịch A. Lấy 300ml dung dịch A cho phản ứng với V lít dung dịch B gồm NaOH 0,2M và KOH 0,29M thu được dung dịch C có pH= 2. Giá trị V là
A.0,214 lít
B. 0,424 lít
C. 0,134 lít
D. 0,414 lít